ELEKTROFYSIK
|
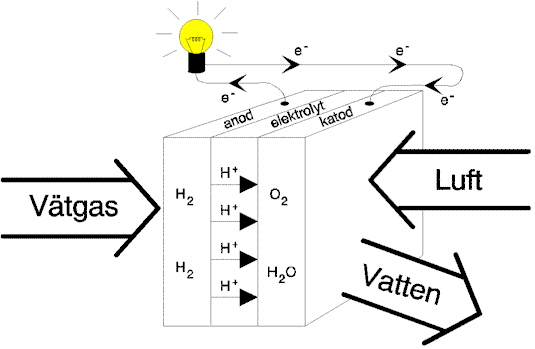
Bränslecellen används för att direkt omvandla kemisk energi (ett bränsle och ett oxidationsmedel) till elektrisk energi. Bränslet utgörs av t.ex. vätgas, metanol eller etanol och oxidationsmedlet är vanligtvis luft. Utsläppen till atmosfären är mycket små. Om bränslecellen drivs av vätgas och luft består avgaserna endast av vatten, se figur nedan. Se en animation av reaktionen i en bränslecell här.
- Cellspänning i vila (teoretiskt) = 1,23 V (ca 0,6 - 1,0 V vid belastning) - Verkningsgrad (teoretiskt) = 83 % (i praktiken 35 - 60 % beroende på typ av bränslecell) - En bränslecell kan skalas ner utan att förlora i verkningsgrad. - Tre huvudtyper av bränsleceller finns: hög-, medel- och lågtemperaturbränsleceller (HT, MT resp. LT). HT-bränsleceller har en god reaktionskinetik men de höga temperaturerna ger stora materialproblem (korrosion). LT-bränsleceller kräver dyra katalytiska elektroder (platina) men har få materialproblem. MT-bränsleceller kan kombinera fördelarna med både HT- och LT-bränsleceller.
|
Redigerad 6/2 2002: I. Albinsson (ialbin@fy.chalmers.se).